- Единицы измерения жесткости воды
- Как повысить жесткость воды в аквариуме?
- Как понизить жесткость воды в аквариуме?
- Как измерить жесткость воды в аквариуме?
- Определение временной, или карбонатной жесткости воды в аквариуме
- Определение общей жесткости воды в аквариуме
- Определение постоянной и карбонатной жесткости с помощью готовых наборов.
- Измерение общей жесткости воды с помощью кондуктометра
Вода – это сложный природный раствор. Вся жизнь на земле зависит от воды и в большей своей части состоит из нее. Вода в том или ином виде содержит в себе, все существующие химические элементы, в том числе и газы. Возможность существования в воде живых существ обусловлена ее гидрохимическими параметрами, которые в свою очередь зависят не только оттого, что в ней содержится, но и в каких пропорциях.
Многие люди слышали о таком понятии как жесткость воды. Но не многие представляют, что это такое и откуда она берется.
Жесткость – это особое свойство воды, во многом определяющее её потребительские качества и поэтому имеющее важное хозяйственное значение. Жесткая вода в процессе кипения образует накипь на стенках всевозможных нагревательных приборов (чайников, отопительных котлов, стиральных машин, батареях и пр.), чем значительно ухудшает их теплотехнические характеристики. Кроме того, жесткая вода плохо подходит для стирки, ухудшая моющие свойства мыла. Катионы Ca2+ и Mg2+ вступают в химическую реакцию с жирными кислотами мыла, в результате которой образуются плохо растворимые соли, создающие пленки и осадки, снижающие качество стирки и повышающие расход моющего средства. Проще говоря, жесткая вода плохо мылится.
Жесткость воды обусловлена содержанием в ней солей кальция и магния. Эти химические элементы являются активными регуляторами многих химических процессов в природе, а жесткость воды несомненно является одним из важнейших показателей качества воды, с какой бы целью она не применялась – для питья, технических нужд, или содержания и разведения рыбы.
Вполне естественно, что вода, взятая из разных водоемов, может существенно отличается по жесткости.
Причем если водоем, будь то озеро или река пополняется водой в основном из подземных источников, которые как правило протекают в известняковых пластах земной коры, при прохождении которых вода обогащается солями жесткости, то вода в таком водоеме будет жесткой.
Если же основной источник пополнения водоема – талая или дождевая вода, то вода в таком водоеме будет мягкой.
В целом, жесткость поверхностных вод, как правило, меньше жесткости вод подземных.
Жесткость воды в природных водоемах периодически изменяется достигая максимального значения в зимний период и минимального весной во время таяния снега. Что касается тропических водоемов, а обитатели аквариумов в основном выходцы из тропических стран, то там наблюдается похожая закономерность. В засушливый сезон вода более жесткая чем в сезон дождей.
Жесткость воды может колебаться в широких пределах. Значительные колебания временной и общей жесткости могут отрицательно сказываться на здоровье обитателей аквариума. Обычно в аквариуме преобладает жесткость, обусловленная наличием ионов кальция (до 70%); однако в некоторых случаях магниевая жесткость может достигать 50-60%. Так например, в озере Танганьика преобладает магниевая жесткость, поэтому иногда аквариумисты практикуют добавление в воду сульфата магния.
Океанская и морская вода имеют очень высокую степень жесткости (десятки и сотни мг-экв/дм3).
Иначе говоря, при незначительном содержании солей кальция и магния, воду называют мягкой, а при большом количестве – жесткой. Кроме этого, также различают кальциевую и магниевую составляющие. Хотя эти элементы довольно близки по своим свойствам, но небольшие различия все же есть. Так, магниевые соли растворяются в воде несколько хуже чем кальциевые, а их избыток придает воде горьковатый вкус.
Итак, жесткость воды это свойство обусловленное содержанием в ней растворимых солей кальция и магния, называемых еще солями жесткости.
Когда речь идет о жесткости воды в аквариуме, то имеется в виду так называемая общая жесткость, образованная двумя составляющими: временной (карбонатной) и постоянной (некарбонатной).
Это соотношение можно записать так:
общая жесткость (GH) = временная жесткость (КН) + постоянная жесткость (NKH).
Временная жесткость отражает наличие в воде гидрокарбонатов магния и кальция. Эти соли легко распадаются в процессе кипячения воды, в результате чего образуется угольная кислота и гидроксид магния с карбонатом кальция в виде осадка, который многим известен как накипь.
От величины временной жесткости зависит растворимость в ней CO2, а соответственно значение pH в аквариуме. Чем выше карбонатная жесткость тем хуже растворяется в воде CO2 и выше значение pH.
Если в аквариуме плохо развиваются растения, то наиболее вероятной причиной этого может быть высокое значение карбонатной жесткости, так как в мягкой воде растения лучше усваивают необходимые им минеральные элементы.
Постоянная жесткость воды в аквариуме обусловлена присутствием в воде кальций-магниевых солей разных кислот (азотной, соляной и серной) и при кипячении не изменяется.
В действующем аквариуме вода со временем смягчается, т.к. кальций усваивается рыбами, беспозвоночными животными и растениями. Поэтому старая вода как правило более мягкая. В аквариуме с большим количеством растений, при сильном освещении, жесткость может, изменятся в течение суток. В дневное время она становиться меньше, а ночью увеличивается. Особенно это актуально для аквариумов, в которых развились зеленые водоросли.
В зависимости от своих свойств вода способствует или тормозит развитию жизненных процессов. В общем случае, для аквариума пригодна чистая, прозрачная, содержащая все необходимые для растений микроэлементы водопроводная вода с GH 5-20°, KH 2-15° градусов, pH 6,5-7,5.
Общая жесткость воды в аквариуме измеряется в GH – это значение показывает суммарное количество в воде ионов щелочноземельных металлов, таких как кальция, магния, стронция, бериллия и бария. Физиологическое значение этих элементов для пресноводных рыб чрезвычайно велико, но потребляют они эти элементы не из воды, а из корма. Строго говоря, в подавляющем большинстве случаев этот параметр для рыб не сильно критичен. Опасность для них представляют только экстремальные значения.
Так, в воде со значением GH близким к нулю вообще ничего живое жить не будет. А при очень больших показателях, превышающих 35-50°GH, в действие вступают уже другие факторы, здесь пресноводная аквариумистика кончается, и начинается зона действия законов природы для солоноватых вод. Тут уже начинают сказываться различные осмотические явления, при которых далеко не каждая пресноводная рыба способна выжить. Во всех же остальных случаях большинство рыб легко адаптируются к любым разумным значениям общей жесткости.
Обратите внимание на взаимосвязь параметров: GH, KH и pH. Хотя эти три параметра различны, они все взаимодействуют друг с другом в разной степени, делая трудным изменение одного параметра без изменения других. Это – одна из причин, по которой начинающим аквариумистам не рекомендуют заниматься изменением параметров воды, если на то нет необходимости.
Как пример, жесткая вода, часто становится из-за известняка. Известняк содержит карбонат кальция, который когда растворяется в воде, увеличивает, и GH (от кальция) и KH (от карбоната). Увеличение KH также обычно увеличивает pH. Как следствие KH действует подобно губке, поглощая кислоту из воды и увеличивая pH.
Единицы измерения жесткости воды
В литературе посвященной аквариумистике, жесткость до сих пор измеряют в градусах, причем в разных странах свои собственные градусы, отличные от других.
Идентичны пожалуй только немецкие и русские градусы жесткости, правда, давно официально отменные в обеих странах, но по-прежнему существующие в аквариумной литературе.
В западных странах используется такие единицы измерения жесткости, как немецкий (d°, dH), французский (f°) и американский градус (ppm CaCO3).
Очень мягкой считается вода с жесткостью от 0 до 4°, мягкой — от 5 до 8°, вода средней жесткости — от 9 до 16°, жесткая вода — от 16 до 30° и более 30° — очень жесткая вода.
Обратите внимание, что сокращения GH, КН и NKH являются общепринятыми во всей аквариумной литературе. Например, вы можете встретить запись 12° dGH и 4° dKH, что означает, соответственно, 12 немецких градусов общей жесткости и 4 немецких градуса карбонатной жесткости.
В городах аквариумисты используют водопроводную воду, жесткость которой зависит прежде всего от географического положения и в меньшей степени от времени года.
Например, жесткость воды в Москве находится в диапазоне от 4 до 12°, в Санкт-Петербурге, от 2 до 3°, а в Одессе 12° и выше.
Для перевода одних градусов жесткости в другие можно воспользоваться таблицей:
| Наименование единиц | мг-экв/л | Немецкий гр. | Французкий гр. | Американский гр. | Английский гр. |
| мг-экв/л | 1 | 2.804 | 5.005 | 50.045 | 3.511 |
| Немецкий гр. | 0.3566 | 1 | 1.785 | 17.847 | 1.253 |
| Французкий гр. | 0.1998 | 0.560 | 1 | 10.000 | 0.702 |
| Американский гр. | 0.0200 | 0.056 | 0.100 | 1 | 0.070 |
| Английский гр. | 0.2848 | 0.79 | 1.426 | 14.253 | 1 |
Как пользоваться этой таблицей?
Допустим, исходная общая жесткость воды в аквариуме равна 3.25 мг-экв/л. Вам надо перевести эту величину в немецкие градусы. В ячейке, соответствующей пересечению строки мг-экв/л и столбца немецких градусов находим коэффициент, он же множитель, равный 2.804. Теперь надо умножить 3.25 на 2.804. Произведение этих чисел и будет жесткостью в немецких градусах (dGH). Жесткость вашей воды в dGH=9.110. То есть, сравнительно с мг-экв/л, немецкие градусы – более мелкие единицы измерения.
Если же вы счастливый обладатель американского теста, и он выдал результат, к примеру, 14 американских градусов (usH), а вам нужны все те же немецкие, то ответ в dGH будет: 14*0.056=0.780. Но это только в том случае, если мы считаем что американский градус равен 1 мг CaCO3 в 1л воды (так пишут во всей русскоязычной литературе), сами же американцы считают, что их градус жесткости в 17.12 раз больше, соответственно, и результат измерения в dGH будет равен 13.35. То есть эти американские градусы довольно близки к немецким.
Пользование разными единицами измерения жесткости без их пересчета может привести к существенному искажению данных. Так 14 американских градусов – это всего лишь 0.78 немецких.
Поэтому читая сообщения американского аквариумиста, о том, что у него рыбы отнерестились при 14° град. жесткости, не думайте, что им подходит для нереста жесткая вода, эта вода на самом деле очень мягкая. В любом случае, первое что надо сделать – это выяснить в каких единицах представлены результаты.
Как повысить жесткость воды в аквариуме?
Для того чтобы повысить жесткость воды в аквариуме на небольшую величину (1-3°) достаточно поместить в него куски мрамора или известняка. В этом случае жесткость воды будет увеличиваться постепенно, причем чем мягче исходная вода, тем быстрее увеличится ее жесткость.
Более эффективный метод повышения жесткости – химический, реализуемый путем добавления в воду растворов хлористого кальция и сульфата магния (магнезии). Эти препараты можно приобрести в аптеке.
Так при добавлении одного миллиграмма 10-процентного раствора хлористого кальция жесткость одного литра воды в среднем повышается на 3°, а добавление одного миллиграмма 25-процентного раствора сульфата магния увеличит жесткость воды на 4°.
Максимальный эффект достигается одновременным использованием обоих препаратов, это даст более близкое к естественному соотношение ионов кальция и магния.
Как понизить жесткость воды в аквариуме?
Существует несколько способов для уменьшения жесткости воды в аквариуме. Самый простой заключается в ее кипячении, например, чтобы уменьшить жесткость воды приблизительно в два раза, необходимо кипятить ее в течение получаса.
Понизить жесткость воды можно путем вымораживания. Этот метод заключается в следующем: воду наливают в небольшой пластиковый контейнер и помещают в холодильник, после того как большая часть воды в емкости замерзнет, не замерзшую воду сливают, а оставшийся лед, практически не содержащий солей, растапливают, после чего доводят температуру полученной воды до комнатной и используют. Полученная таким способом вода будет иметь значительно меньшую жесткость.
Оба этих метода понижения жесткости рассчитаны на не большие объемы воды. А как быть в случае если необходимо уменьшить жесткость воды в большом аквариуме?
В этом случае, для получения мягкой воды используют специальное оборудование.
На сегодняшний день лучшим решением можно считать использование установки обратного осмоса. Такие установки (фильтры) вполне доступны и используются в бытовых целях. На выходе такого фильтра вода будет иметь нулевую жесткость.
А для получения воды определенной жесткости достаточно разбавить отстоянную водопроводную воду полученной водой.
Объем необходимой водопроводной воды, можно рассчитать по формуле:

GH’ — необходимая жесткость воды
V’ — объем воды с необходимой жесткостью
GH — жесткость водопроводной воды
А чтобы найти объем «осмолята» нужно просто вычесть объем водопроводной воды из объема воды с необходимой жесткостью:

Например, чтобы получить 60 литров воды с жесткостью 4 градуса, при жесткости воды в водопроводе 15 градусов:

Нужно взять 16л водопроводной воды и смешать ее со следующим объемом «осмолята»: Vосм=60л–16л=44л
Для устранения жесткости также используется метод ионного обмена или катионирования, когда воду пропускают через слой катионита (специальной смолы). При этом катионы Са2+ и Mg2+, находящиеся в воде, обмениваются на катионы Nа+, содержащиеся в применяемом катионе. В некоторых случаях требуется удалить из воды не только катионы Са2+ и Mg2+, но и другие катионы и анионы. В таких случаях воду пропускают через катионит, содержащий в обменной форме водородные ионы (Н – катионит), и анионит, содержащий гидроксид – ионы (ОН – анионит).
В итоге вода освобождается как от катионов, так и от анионов солей. Такая обработка воды называется ее обессоливанием.
Как измерить жесткость воды в аквариуме?
Оценить значение общей жесткости воды в аквариуме можно по крайней мере шестью различными способами:
1. Комплексонометрическим титрованием трилоном Б. Это самый точный метод, но не самый простой.
2. С помощью покупных тестов. Это не очень точно, зато быстро и просто.
3. С помощью измерения электропроводности воды. Очень просто, но нужен кондуктометр.
4. С помощью ионометра (вольтметра с высоким входным сопротивлением) и ионоселективного электрода.
5. С помощью титрования соляной кислотой пробы воды, обработанной щелочью и содой. Это не просто и не очень точно.
6. С помощью обычного хозяйственного мыла. Это тоже не точно, но и не сложно.
Определение временной, или карбонатной жесткости воды в аквариуме
Определение карбонатной жесткости воды проводится путем её титрования соляной кислотой.
Под титрованием понимается добавление к исследуемой воде раствора реагента, концентрация которого заранее известна. По расходу этого реагента, а он вступает в химическую реакцию с тем веществом, содержание которого хотят определить, рассчитывают концентрацию определяемого вещества.
Для аквариумных нужд удобно пользоваться 0.05М раствором соляной кислоты. В качестве индикатора понадобится метиловый оранжевый, который необходим для того, чтобы установить момент окончания титрования.
Соляная кислота, и метиловый оранжевый очень распространенные реактивы. Их всегда можно приобрести в специализированных магазинах. Присутствуют они и в любой химической лаборатории.
Приготовление реактивов:
Для приготовления 0.05М раствора соляной кислоты, 4 мл покупной 38% соляной кислоты растворяют в дистиллированной воде (примерно в 200-300 мл), после чего доводят все той же водой раствор до 1 литра.
Работа с концентрированной соляной кислотой требует предельной осторожности, ОНА НЕ ДОЛЖНА ПОПАДАТЬ НА РУКИ И ОДЕЖДУ, а ВДЫХАНИЕ ЕЕ ПАРОВ ВРЕДНО. Помните, что ВСЕГДА НАДО ДОБАВЛЯТЬ КИСЛОТУ В ВОДУ, А НЕ ВОДУ В КИСЛОТУ.
Разбавленная до указанной концентрации соляная кислота никакой опасности не представляет.
Для приготовления раствора индикатора небольшое его количество — 0.1 г растворяют в 100 мл дистиллированной воды. Особой точности здесь не требуется, все можно сделать на глаз.
Проведение анализа:
Как можно точнее отмеряют 50 мл исследуемой воды. Добавляют в нее несколько капель раствора метилового оранжевого, до тех пор пока вода не окрасится в желтый цвет. Далее проводят титрование пробы кислотой до изменения цвета индикатора.
Кислоту удобно набрать в шприц до отмеченного заранее деления и из него дозировано добавлять в раствор. Сначала порции кислоты могут быть относительно большими, но к концу титрования надо быть аккуратным и осторожным, цвет может поменяться буквально от одной капли.
Титровать надо не торопясь, осторожно перебалтывая воду в стаканчике.
Как только цвет раствора изменится с желтого на оранжевый, следует прекратить титрование. Лучше проделать эту процедуру несколько раз, каждый раз точно засекая какой объем кислоты был израсходован.
Затем вычислить СРЕДНИЙ ОБЪЕМ пошедшей на титрование кислоты. Зная этот объем можно рассчитать карбонатную жесткость по формуле:

Где Ск — концентрация кислоты в молях (М/л), Vк — объем раствора кислоты использованный при титровании (мл), Vв — объем пробы воды, взятой для титрования (мл).
Если Ск = 0.05 М, а Vв = 50 мл, то

То есть если вы титровали 50 мл воды 0.05 М соляной кислотой, то в этом случае карбонатная жесткость в
мг-экв/л будет численно равна объему кислоты (в мл), израсходованному для титрования.
Например, если на титрование ушло 1.5 мл раствора кислоты, то карбонатная жесткость воды равна 1.5 мг-экв/л. Для перевода в градусы KH значение в мг-экв/л надо умножить на 2.804: 1.5*2.804=4.2°KH.
Определение общей жесткости воды в аквариуме
Этот тест не отличается от большинства других тестов для определения общей жесткости, он основан на титровании кальция и магния трилоном Б в присутствии металлоиндикатора. В качестве индикатора в данном случае используется хром темно-синий, который позволяет определить кальций и магний отдельно.
Приготовление реактивов.
Индикатор: В 10 мл этилового спирта на кончике ножа внести индикатор (хром темно-синий), порошок растворяется долго. Раствор должен быть темный, как крепкий раствор марганцовки. При отсутствии спирта можно использовать водку.
Титровальный раствор: 500 мг трилона Б (динатриевой соли ЭДТА 2-водной) растворить в 75 мл дистиллированной воды.
Определение общей жесткости (суммы кальция и магния)
К 10 мл исследуемой воды добавить 8-10 капель 10%-ного раствора аммиака (аптечного нашатырного спирта) для создания щелочной среды и 1-3 капли индикатора до появления хорошо заметной розово-сиреневой окраски.
Затем по каплям добавлять раствор трилона Б до появления устойчивой сине-фиолетовой окраски, перемешивая пробу после каждой капли. При приближении к конечной точке титрования добавлять титровальный раствор следует медленно, так как смена окраски может произойти через 2-3 секунды после добавления очередной капли.
Результат получаем в немецких градусах: 1 капля = 0,5 dGH (для пипетки 1 мл=20 капель), т.е. если на титрование ушло 20 капель, то общая жесткость GH=10.
Определение постоянной и карбонатной жесткости с помощью готовых наборов.
Такие тесты выпускаются многими производителями, они продаются в зоомагазинах.
Пользоваться ими просто и удобно. Как правило такие наборы продаются в красивой упаковке в которой находятся: мерный стаканчик, пузырек-капельница с реагентом-индикатором и инструкция.
Ход анализа предельно прост.
Для определения общей жесткости:
В мерный стаканчик надо набрать 5 мл исследуемой воды, далее в достаточно освещенном помещении, поместив стаканчик против белого фона, добавляем содержимое теста по каплям, перемешивая после каждой капли, до тех пор, пока вода не изменит цвет с розового на зеленый. Количество капель соответствует значению общей жесткости воды в немецких градусах.

Для определения карбонатной жесткости:
В 5 мл. исследуемой воды добавляем содержимое теста по каплям, перемешивая после каждой капли, до тех пор, пока вода не изменит цвет с синего на желтый. Число капель соответствует значению карбонатной жесткости воды в немецких градусах.

Вы не пожалеете если приобретете эти наборы.
Измерение общей жесткости воды с помощью кондуктометра
Кондуктометр (TDS-метр) — это электронный прибор, измеряющий электропроводность воды, которая тем выше, чем больше в ней растворено солей. Поэтому его еще иногда называют солемер.

Этот метод позволяет составить достаточно точное представление о жесткости воды в аквариуме в том случае, если Вы не сыпали в аквариум поваренную соль и не регулировали рН средствами типа рН-минус, рН-плюс и другими кислотами и щелочами.
По его показаниям можно косвенно судить о величине общей жесткости, для этого достаточно лишь воспользоваться графиком
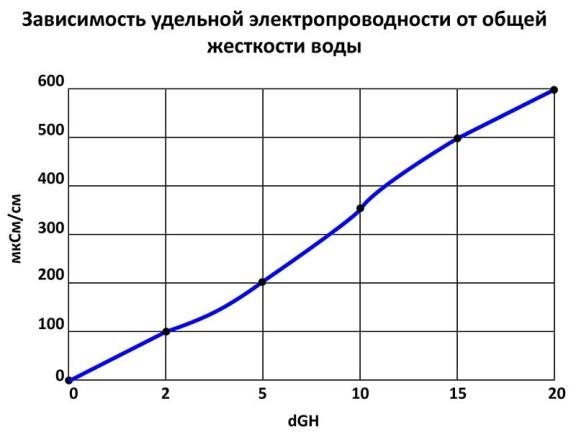
Объяснять тут почти совсем нечего – все очень просто.
Если электропроводность воды, к примеру, 200 мкСм/см, то жесткость ее будет около 5° dGH, если — 360 мкСм/см, то около 10° dGH и т.д. Можно распечатать этот график и проведя горизонтальную линию от точки на оси ординат, соответствующей значению электропроводности, до пересечения ее с кривой графика, а от этой точки вертикальную линию до оси абсцисс, определить общую жесткость воды. График этот составлен на основе анализа реальных образцов природных вод.
Метод подкупает своей простотой. Но при его использовании необходимо учитывать, что это косвенное измерение общей жесткости.
Показания прибора сильно зависят от температуры исследуемого раствора (существуют модели с термокомпенсацией, но они дороже). А так же электропроводность зависит от активной реакции воды(pH). При длительном использовании возможна сульфатация электродов, которая так же искажает показания прибора (есть модели, в которых для измерения используется переменный ток, но они так же дороже).
При соблюдении рекомендаций производителя, необходимости частых быстрых замеров и возможности периодически контролировать показания прибора более точными методами, подобный прибор просто не заменим.
Самым доступным, дешевым и точным в домашних условиях, без использования сложного химического или электронного оборудования является метод определения общей жесткости с помощью обычного хозяйственного мыла.

Этот способ описал в своей книге И. Шереметьев. Основан этот метод на том, что хозяйственное мыло, как и любое другое трудно размылить в жесткой воде. И только когда мыло свяжет избыток солей кальция и магния – появляется мыльная пена.
Для определения жесткости воды нужно взвесить один грамм хозяйственного мыла, измельчить его и аккуратно, чтобы не образовалась пена растворить в небольшом количестве горячей дистиллированной воды. Дистиллированную воду можно купить в автомагазинах. Она используется для добавления в аккумулятор при повышении концентрации электролита.
Далее мыльный раствор наливаем в цилиндрический стакан и доливаем дистиллированной воды до уровня 6 сантиметров, если мыло 60% или до уровня 7 сантиметров если мыло 72%. Процент содержания мыла указан на бруске. Теперь в каждом сантиметре уровня мыльного раствора содержится количество мыла способное связать соли жесткости, количество которых соответствует 1°dH в 1 литре воды.
Далее в литровую банку наливаем пол-литра исследуемой воды. И непрерывно помешивая, понемногу прибавляем наш мыльный раствор из стакана в банку с исследуемой водой. Поначалу на поверхности будут только серые хлопья. Затем появятся разноцветные мыльные пузыри. Появление устойчивой белой мыльной пены говорит о том, что все соли жесткости в исследуемой воде связаны.
Теперь смотрим на наш стакан и определяем, сколько сантиметров раствора нам пришлось вылить из стакана в исследуемую воду. Каждый сантиметр связал в половине литра воды количество солей соответствующее 2°dH. Таким образом, если вам пришлось до появления пены вылить в воду 4 сантиметра мыльного раствора, то жесткость исследуемой воды равна 8°dH.
Если вы вылили в воду весь мыльный раствор, а пена так и не появилась, это означает, что жесткость исследуемой воды больше 12°dH. В таком случае исследуемую воду разбавляем дистиллированной водой в два раза. И проводим анализ снова. Теперь полученный результат жесткости нужно будет умножить на два. Полученное значение будет соответствовать жесткости исследуемой воды.
При определенном опыте погрешность метода около 1 – 2 °dH. Что вполне допустимо для наших целей. Учитывая простоту и доступность метода он, безусловно, заслуживает внимания.
Вообще-то, большинство рыб и растений способны благополучно приспосабливаться к изменяющимся условиям, в том числе и к непривычной жёсткости (или, наоборот, мягкости) воды.
Умение различать такие параметры воды, как жесткость и мягкость, необходимо в том случае, если вам придется иметь дело с каким-нибудь “трудным” видом рыб, предъявляющим высокие требования к окружающей среде. Но размножение рыбы в условиях неподходящей жёсткости весьма затруднительно, а иногда и совершенно невозможно. При выборе рыб и растений для вашего аквариума вы обязаны учитывать их требования к жесткости воды.
Например, совершенно недопустимо сажать вместе цихлид из африканских озер Малави и Танганьика, которым нужна жесткая вода, и рыб из бассейна реки Амазонки, которым нужна мягкая вода.
Вам необходимо заранее определиться со своими пристрастиями и решить, какая жесткость воды будет в вашем аквариуме и соответственно, какие рыбы будут у вас жить.
Водные растения, достаточно чувствительные к жесткости воды, предпочитают слабожесткую, хотя есть и исключения. Так, мадагаскарские апоногетоны решетчатые, баивианус растут в водах с жесткостью 0,8-1,2°dH, а в аквариумах погибают при жесткости 4-5°. Криптокорина цилиата, наоборот, растет при жесткости, превышающей 20-30°.
Поскольку развитие растений в очень мягкой воде попросту невозможно, для большинства аквариумистов вопрос об этом типе воды не возникает вне зависимости от того, можно его воспроизвести или нет.
В мягкой воде разрушаются раковины улиток, плохо переносят линьку креветки и раки – этим животным недостает кальция.
Большинство аквариумных рыб и растений на своей родине живет в очень мягкой или мягкой воде. В наших кранах в среднем течет вода средней жесткости или жесткая. Но не стоит отчаиваться – благодаря тому, что рыбы и растения живут в аквариумах не первый год – они адаптировались к повышенной жесткости. Это касается “нетребовательных” рыб и растений – если же Вы хотите завести требовательные к мягкой воде живые организмы, то Вам придется смягчать воду.
Большинство аквариумных рыб, содержащихся в аквариуме, нормально живут при 3-15° жесткости. Но и здесь мы встречаемся с отклонениями. Живородящие рыбки нуждаются в воде с жесткостью 10-15° dH, харациниды предпочитают 3-6° dH, цихлиды озера Малави – 14-20° dH. Некоторые бычки из рек Азии в мягкой воде очень быстро погибают.
Жесткость – важный параметр для аквариумиста, однако стоит особо отметить, что это свойство воды определяется только количеством некоторых растворенных в ней минеральных веществ. Есть и другие химические элементы, вносящие вклад в общее содержание минеральных веществ, но не влияющие на жесткость воды, и которые можно измерить с помощью специальных тестов.
Очень важно помнить об этом, так как некоторые методы смягчения воды не снижают содержания минеральных веществ, а просто превращают соли, делающие воду жесткой, в другие соли, не влияющие на жесткость.





